Механизм работы рецепторов сопряженных с G-белком. Каталитический домен имеет центр, связывающий АТФ и белок-субстрат
Групп C и G. Белок G имеет сходства с белком А, но отличается специфичностью. Белок G имеет молекулярную массу 58 кДа (в случае белка C40) или 65 кДа (в случае белка G148). Белок G связывается с -регионом антител и поэтому находит широкое применение для очистки иммуноглобулинов. Молекулы белка G также связывают альбумин .
Другие белки, связывающие иммуноглобулины
Существуют и другие бактериальные белки, связывающие иммуноглобулины, - белок A, белок A/G и белок L. Эти белки используют для очистки, иммобилизции и выделения иммуноглобулинов. Эти белки, связывающие антитела, имеют различные профили связывания иммуноглобулинов.
См. также
Ссылки
- http://www.jbc.org/cgi/reprint/266/1/399 Sjobring U, Bjorck L, Kastern W, Streptococcal protein G. Gene structure and protein binding properties, J Biol Chem. 1991 Jan 5;266(1):399-405
Wikimedia Foundation . 2010 .
Смотреть что такое "Белок G" в других словарях:
- (англ. protein A) это белок, молекулярной массой 40 60 кДа, выделенный с поверхности клеточной стенки золотистого стафилококка (Staphylococcus aureus). Белок А используется в биохимических исследованиях, так как хорошо связывает многие… … Википедия
Вытаращить арабские белки.. Словарь русских синонимов и сходных по смыслу выражений. под. ред. Н. Абрамова, М.: Русские словари, 1999. белок глобулин, гистон, протеиноид, протеин, протеиновое тело, протамин, протеид Словарь русских синонимов … Словарь синонимов
Толковый словарь Ушакова
1. БЕЛОК1, белка, муж. (биол. хим.). Важнейшая составная часть организма животных и растений; то же, что альбумин и белковина. 2. БЕЛОК2, белка, муж. 1. Выпуклая непрозрачная оболочка глаза. || только мн. Глаза (прост.). Белки выпучить. Белками… … Толковый словарь Ушакова
1. БЕЛОК1, белка, муж. (биол. хим.). Важнейшая составная часть организма животных и растений; то же, что альбумин и белковина. 2. БЕЛОК2, белка, муж. 1. Выпуклая непрозрачная оболочка глаза. || только мн. Глаза (прост.). Белки выпучить. Белками… … Толковый словарь Ушакова
белок C - Белок, сериновая протеаза, синтезируемая клетками печени; антикоагулянт, является ингибитором факторов Va и VIIIa свертывания крови; частота гетерозигот по дефициту Б.C в популяциях человека достигает 1/200 данная аномалия связана с повышенным… … Справочник технического переводчика
БЕЛОК, органическое СОЕДИНЕНИЕ, содержащее множество АМИНОКИСЛОТ, соединенных ковалентными пептидными связями. Молекулы белков состоят из по липептидных цепей. В живых КЛЕТКАХ имеется около 20 различных аминокислот. Из за того, что в каждой… … Научно-технический энциклопедический словарь
БЕЛОК, лка, муж. Высокомолекулярное органическое вещество, обеспечивающее жизнедеятельность животных и растительных организмов. | прил. белковый, ая, ое. Белковые корма (с высоким содержанием белка). II. БЕЛОК, лка, муж. 1. Прозрачная часть яйца … Толковый словарь Ожегова
Белок, связывающий жирные кислоты Белки, связывающие жирные кислоты (англ. fatty acid binding proteins, FABP; БСЖК) семейство транспортеров жирных кислот и других липофильных веществ, таких как эйкозаноиды и ретиноиды. Как считается, эти… … Википедия
1. БЕЛОК, лка; м. 1. Прозрачная жидкость, окружающая желток птичьего яйца. / О такой части куриного яйца как пище. Выпить сырой б. Взбитые белки. ◁ Белковый, ая, ое. Б. крем (из яичных белков). 2. БЕЛОК см. 1. Белки. 3. БЕЛОК см. 2. Белки. 4.… … Энциклопедический словарь
Среди органических веществ белки , или протеины , - самые многочисленные, наиболее разнообразные и имеющие первостепенное значение биополимеры. На их долю приходится 50 - 80% сухой массы клетки.
Молекулы белков имеют большие размеры, поэтому их называют макромолекулами . Кроме углерода , кислорода , водорода и азота , в состав белков могут входить сера, фосфор и железо. Белки отличаются друг от друга числом (от ста до нескольких тысяч), составом и последовательностью мономеров. Мономерами белков являются аминокислоты (рис. 1)
Бесконечное разнообразие белков создается за счет различного сочетания всего 20 аминокислот. Каждая аминокислота имеет свое название, особое строение и свойства. Их общую формулу можно представить в следующем виде:

Молекула аминокислоты состоит из двух одинаковых для всех аминокислот частей, одна из которых является аминогруппой (-NH 2 ) с основными свойствами, другая - карбоксильной группой (-COOH ) с кислотными свойствами. Часть молекулы, называемая радикалом (R ), у разных аминокислот имеет различное строение. Наличие в одной молекуле аминокислоты основной и кислотной групп обусловливает их высокую реакционную способность. через эти группы происходит соединение аминокислот при образовании белка. При этом возникает молекула воды, а освободившиеся электроны образуют пептидную связь. Поэтому белки называют полипептидами .
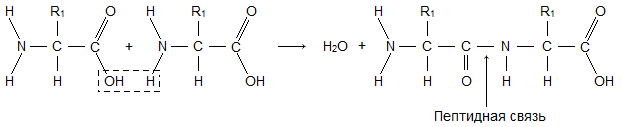
Молекулы белков могут иметь различные пространственные конфигурации, и в их строении различают четыре уровня структурной организации.
Последовательность аминокислот в составе полипептидной цепи представляет первичную структуру
белка. Она уникальна для любого белка и определяет его форму, свойства и функции.
Большинство белков имеют вид спирали в результате образования водородных связей между -CO-
и -NH-
группами разных аминокислотных остатков полипептидной цепи. Водородные связи малопрочные, но в комплексе они обеспечивают довольно прочную структуру. Эта спираль - вторичная структура
белка.
Третичная структура - трехмерная пространственная «упаковка» полипептидной цепи. В результате возникает причудливая, но для каждого белка специфическая конфигурация - глобула . Прочность третичной структуры обеспечивается разнообразными связями, возникающими между радикалами аминокислот.
Четвертичная структура
характерна не для всех белков. Она возникает в результате соединения нескольких макромолекул с третичной структурой в сложный комплекс. Например, гемоглобин крови человека представляет комплекс из четырех макромолекул белка.
Такая сложность структуры белковых молекул связана с разнообразием функций, свойственных этим биополимерам.
Нарушение природной структуры белка называют денатурацией
. Она может происходить под воздействием температуры, химических веществ, лучистой энергии и других факторов. При слабом воздействии распадается только четвертичная структура, при более сильном - третичная, а затем - вторичная, и белок остается в виде полипептидной цепи.
Этот процесс частично обратим: если не нарушена первичная структура, то денатурированный белок способен восстанавливать свою структуру. Отсюда следует, что все особенность строение макромолекулы белка определяются его первичной структурой.
Кроме простых белков , состоящих только из аминокислот, есть еще и сложные белки
Гуанидиннуклеотидсвязывающие регуляторные белки, или G– белки, ответственны за передачу сигналов множества гормонов или нейромедиаторов к разнообразным мишеням клетки. ЧетыреG– белка были очищены до гомогенного состояния и биохимически охарактеризованы:G t (трансдуцин),G s ,G i иG o . Оказалось, что каждый из них имеет уникальные мишени или эффекторные белки.G t активирует сGMP– специфическую фосфодиэстеразу в наружных сегментах палочек сетчатки;G s иG i соответственно стимулируют и ингибируют аденилатциклазу и присутствуют во всех клетках;G o представлен в большом количестве в клетках мозга и, по – видимому, ингибирует электрочувствительный Са 2+ - канал в нейронах. Кроме того, почти, несомненно, имеются и другие пока не выделенныеG– белки.G– белокG p , вероятно, использует в качестве мишени фосфатидилионозитолспецифичную фосфолипазу С, которая инициирует быстрый распад фосфатидилинозиола в плазматической мембране и образование нескольких вторичных посредников. Существует белокG k , который, по – видимому, открывает К + - специфические каналы в сердечной мышце и в других клетках.G– белки внутри клетки могут отвечать на связывание лиганда с одним из нескольких рецепторов. Они могут иметь больше одной мишени.
Все четыре выделенных белка являются αβγ – гетеротримерами. У них довольно большие различия между субъединицами. Имеются, например, три α – субъединицы. β – субъединиц пока известно, как минимум 2. Имеются также сведения, что существенные различия обнаружены и в γ – субъединицах. α – субъединицы связывают GTPи обладаютGTPазной активностью при отсоединении от βγ – субъединичной пары. α - Субъединица также содержит сайт, по которому может происходить АDP– рибозилирование бактериальными экзотоксинами.G i ,G o иG t (трансдуцин) модифицируются коклюшным токсином, аG s иG t – холерным токсином. Эта ковалентная модификация блокирует фосфорилированиеG– белка и служит одним из тестов на участиеG– белков в качестве интермедиатов в клеточных ответах.
Все G– белки прочно связаны с плазматической мембраной, за исключением трансдуцина. Ни одна из субъединиц не является трансмембранным белком.
Обновление фосфатидилинозитола и вторичные посредники
Наиболее широкораспрастранёнными мишенями G– белков являются аденилатциклаза (дляG s иG i) и фосфолипаза С, ответственная за гидролиз фосфатидилинозитола (дляG p). Модуляция аденилатциклазы приводит к изменению внутриклеточной концентрации сАМР, которая, как известна, служит вторичным посредником, влияя на множество внутриклеточных процессов. Одним из последствий увеличения содержания сАМР является, например, стимуляция сАМР – зависимой протеинкиназы (протеинкиназа А), которая в свою очередь фосфорилирует специфические белковые субстраты. Клетки содержат также два типа Са 2+ - зависимых протеинкиназ, активируемых соответственно Са 2+ - кальмодулином и Са 2+ вместе с диацилглицеролом и фомфатидилсерином (протеинкиназаС). Активность обоих киназ регулируется вторичными посредниками, образующими при деградации фосфатидилинозитола, которая во многих клетках инициируется путемG– белокзависимой активации специфической фосфолипазы С.
На долю фосфатидилинозитола приходится лишь 2 – 8% всех фосфолипидов, содержащихся в клеточных мембранах эукариотов. Структура полярной головки представлена миоинозитолом. Данное соединение впервые было выделено из мышц. Небольшая часть фосфотидилинозитола фосфорилирована по положению 4 или по положениям 4 и 5. От 1 до 10% фосфатидилинозитола, присутствующего в мембране, приходится на долю фосфотидилинозитол(4,5) – бифосфата. Этот компонент является, вероятно, первой мишенью для фосфотидилинозитолспецифичной фосфолипазы С, которая активируется во многих клетках G– белком. Последующий гидролиз приводит к быстрому распаду фосфатидилинозитола в плазматической мембране и кратковременному возрастанию количества продуктов распада. Продукты распада действуют как вторичные посредники и участвуют во многих клеточных процессах. Исследование этой системы ещё не закончено, но последовательность событий такова:
Начальными продуктами гидролиза фосфотидилинозитол(4,5) – бифосфата являются диацилглицерол и инозитол (1,4,5) – трифосфат. Диацилглицерол связан с мембраной, а инозитол(1,4,5) – трифосфат является растворимым компонентом. Обычно жирные кислоты фосфотидилинозитола представлены стеариновой в положении 2 и арахидоновой кислотой в положении 2 глицерола.
Инозитол(1,4,5) – трифосфат служит вторичным посредником, и его основной функцией, по – видимому, является мобилизация Са 2+ , аккумулированного в эндоплазматическом ретикулуме. Возможно, этот компонент путём прямого связывания открывает Са 2+ - специфичные каналы в ЭПР, что приводит к увеличению концентрации Са 2+ в цитоплазме в несколько раз. Обычно концентрация свободного кальция в цитоплазме составляет 0,1 мкМ.
Специфичная киназа превращает некоторое количество инозитол(1,4,5) – трифосфата в тетрафосфорилированный продукт (инозитол(1,3,4,5) – тетрафосфат). Образуются также другие, в том числе циклические фосфоинозиды, и некоторые из них имеют определённое физиологическое значение.
Одним из ферментов, регулируемых Са 2+ , является фосфолипаза С, которая при низкой концентрации кальция использует в качестве субстрата фосфотидилинозитол(4,5) – бифосфат, но при более высокой концентрации кальция использует нефосфорилированный фосфатидилинозитол. Возможно, это облегчает непосредственный быстрый гидролиз основной части фосфатидилинозитола.
Наиболее важным ферментом является протеинкиназа С. этот фермент локализован преимущественно в цитозоле до момента появления там диацилглицерола и Са 2+ . Затем в зависимости от присутствия фосфотидилсерина он связывается с плазматической мембраной и активируется. Эффекты сходные с действием диацилглицерола, оказывают форболовые эфиры, и протеинкиназу С часто рассматривают как рецептор этих соединений. В активированном состоянии протеинкиназа С является серин – и треонинспецифичной протеинкиназой, которая фосфорилирует как специфические мишени, так и саму себя. Механизм регуляции работы протеинкиназы С неизвестен; установлено лишь, что ганглиозиды и лизосфинголипиды ингибируют этот фермент, а, кроме того, ещё и выделен ингибитор белковой природы.
Дацилглицерол может подвергаться дальнейшей деградации под действием диацилглицероллипазы до арахидоновой кислоты, которая окисляется до множества биологически активных метаболитов, называемых эйкозаноидами и включающих простагландины. Хотя сама арахидоновая кислота является вторичным посредником, неясно, насколько существенен для её образования фосотидилинозитолспецифичный, зависимый от фосфолипазы С путь. Арахидоновая кислота может образовываться из множества фосфолипидов при действии фосфолипазы А 2 . В некоторых типах клеток путь биосинтеза с участием фосфолипазы А 2 более важен.
Исходя из вышесказанного, можно утверждать, что при функционировании этой системы образуются, по меньшей мере, три известных вторичных посредника: диацилглицерол, инозитол(1,4,5) – трифосфат и арахидоновая кислота. Каждый из этих посредников выполняет специфические функции, включая увеличение содержания внутриклеточного кальция и активацию кальций – зависимых протеинкиназ.
Сигнальные G-белки являются универсальными посредниками при передаче гормональных сигналов от рецепторов клеточной мембраны к эффекторным белкам , вызывающим конечный клеточный ответ.
Они являются объектом интенсивного изучения в связи с их участием во многих важных физиологических процессах (см. обзоры Gilman, 1987 ; Neer, Clapham, 1988 ; Freissmuth et al.,1989 , Кухарь В.П. ea, 1992). G-белки, участвующие в передаче сигнала, являются членами большого надсемейства гуанин-связывающих белков. G- белки - это прецизионные регуляторы, включающие или выключающие активность других молекул.
Связывание агониста (гормона, нейромедиатора и др.) с соответствующим рецептором приводит к белок-белковому взаимодействию между рецептором и G-белком и ускоряет диссоциацию ГДФ. В результате образуется короткоживущий комплекс агонист - рецептор - G-белок, не связанный ни с каким нуклеотидом. Связывание с этим комплексом молекулы ГТФ снижает сродство рецептора к G-белку, что приводит к диссоциации комплекса и высвобождению рецептора. Потенциально рецептор может активировать большое количество молекул G-белка, обеспечивая, таким образом, высокий коэффициент усиления внеклеточного сигнала на данном этапе. Активированная альфа-субъединица G-белка (альфа* ГТФ Мg). [ Bourne, ea 1997 ] диссоциирует от бета-гамма-субъединиц и вступает во взаимодействие с соответствующим эффектором, оказывая на него активирующее или ингибирующее воздействие.
Альфа-субъдиница с присоединенным с ней ГТФ способна взаимодействовать с эффектором в мембране - ферментами, такими, как аденилатциклаза , или, возможно, ионными каналами . Фермент может активироваться или ингибироваться, а ионный канал - открываться или закрываться. Конкретные примеры будут рассмотрены в последующих главах. Взаимодействие с эффектором, однако, длится до тех пор, пока альфа- субъединица, являющаяся ГТФ-азой, удерживает ГТФ. Так что, очень вскоре присоединенный ГТФ гидролизуется до ГДФ. Когда это происходит, альфа- субъединица снова меняет свою коонформацию и теряет способность активировать эффектор. После этого альфа-ГДФ взаимодействует с бета- гамма-комплексом и снова образует тримерный комплекс, завершая, таким образом, цикл ( рис. 1.9). Предполагают также, что комплекс из бета-гамма-субъединиц тоже может (прямо или опосредованно) влиять на эффекторные фермент ы.
Впоследствии ГТФ, связанный с альфа-субъединицей G-белка, подвергается гидролизу, причем ферментом, катализирующим этот процесс, является сама альфа-субъединица . Это приводит к диссоциации альфа-субъединицы от эффектора и реассоциации комплекса альфаГДФ с бета-гамма-субъединицами. Спонтанная активация G-белка, связанного с ГДФ - весьма маловероятный процесс.
Этот же механизм лежит в основе гормональной регуляции фосфоинозитид-специфичной фосфолипазы С ( Boyer et al., 1989) и фосфолипазы А 2 ( Axelrod et al., 1988). Кроме того, было показано, что G белки могут непосредственно активировать ионные каналы ( Sternweis, Pang, 1990). см. также:
Лимитирующей стадией процесса восстановления исходного состояния G-белка является скорость диссоциации GDP от альфа-субъединицы G-белка. Скорость диссоциации увеличивается при взаимодействии G-белок-GDP с агонист-связанным рецептором [ Branot D.R.,1986 ]. Связывание GTP G-белком приводит, очевидно, к образованию комплекса агонист-рецептор-G-белок. Аналог GTP-CTP-гамма-S и Mg 2+ усиливает диссоциацию альфа-субъединицы из тримера G-белка [ Northup J.V.,1983 ]. Однако следует заметить, что каталитическая субъединица аденилатциклазы из мембран мозга быка хроматографически соочищается с альфа- и бета-субъединицами G S -белка [ Marbach J.,1990 ] и вопрос диссоциации альфа-субъединиц из тримера G-белка для активации эффектора требует уточнения.
G-белки проявляют значительный полиморфизм. Каждая из форм субъединиц G-белка высокогомологична по структуре, близка по функциям, но отличается молекулярной массой и электрофоретической подвижностью [ Перцева М.Н.,1990 ]. Особенно широк полиморфизм и наиболее изучен для альфа s и альфа i G-белков. Так из мозга человека выделено 11 форм сДНК, ответственных за синтез альфа s субъединиц, четыре вида которых клонированы и, предполагается, что они определяют синтез четырех изоформ альфа s в мозге человека [ Bray P.,1986 ]. Для альфа i найдены, в основном, три изоформы альфа i 1, альфа i 2, альфаi 3 . Молекулярные массы изоформы альфаs находятся в пределах 42-55 кДа, а альфаi -39-41 кДа [ Перцева М.Н.,1990 ]. Распределение молекулярных вариантов альфаi носит тканеспецифический характер: альфа i 1 представлена, в основном, в мозге, альфа i 2 обнаружена в нервной ткани и в клетках крови, альфаi 3 представлена в переферических тканях и отсутствует в мозге [ ; Itoh I.,1988 ]. Что касается изоформ альфа-субъединиц G s -белков, то пока неясно, кодируются ли изоформы разными структурными генами или это продукт одного гена с последующим внутренним альтернативным сплайсингом исходного РНК-транскрипта [ Robishaw J.D.,1986 ], или множественность их результат посттрансляционной модификации [ Casey P.J.,1988 ]. В настоящее время известно 9 структурных генов, кодирующих C-белки и 12 продуктов этих генов [
G-белки (ГТФ-связывающие белки) - универсальные посредники при передаче сигналов от рецепторов к ферментам клеточной мембраны, катализирующим образование вторичных посредников гормонального сигнала. G-белки - олигомеры, состоящие из α, β и γ-субъединиц. Состав димеров βγ незначительно различаются в разных тканях, но в пределах одной клетки все G-белки, как правило, имеют одинаковый комплект βγ-субъединиц. Поэтому G-белки принято различать по их α-субъединицам.. Выявлено 16 генов, кодирующих различные α-субъединицы G-белков. Некоторые из генов имеют более одного белка, вследствие альтернативного сплайсинга РНК.
Каждая α-субъединица в составе G -белка имеет специфические центры:
Связывания ГТФ или ГДФ;
Взаимодействия с рецептором;
Связывания с βγ-субъединицами;
Фосфорилирования под действием протеинкиназы С;
Взаимодействия с ферментом аденилатциклазой или фосфолипазой С.
В структуре G -белков отсутствуют α-спиральные, пронизывающие мембрану домены. G -белки относят к группе «заякоренных» белков (рис. 5-34).
Рис. 5-34. Положение G-белков в мембране. Для ассоциации G-белков важно ацилирование α-протомеров алифатическими радикалами жирных кислот, миристиновой кислоты (М) или изопреновой. γ-Субъединица G-белка имеет геранил-геранильную группу (Г), связанную тиоэфирной связью с остатком цистеина С-конца.
Регуляция активности G -белков
Различают неактивную форму G -белка - комплекс αβγ-ГДФ и активированную форму αβγ -ГТФ. Активация G-белка происходит при взаимодействии с комплексом активатор-рецептор, изменение конформации G-белка снижает сродство α-субъединицы к молекуле ГДФ и увеличивает к ГТФ. Замена ГДФ на ГТФ в активном центре G-белка нарушает комплементарность между α-ГТФ и βγ-субъединицами. Рецептор, связанный с сигнальной молекулой, может активировать большое количество молекул G-белка, таким образом обеспечивая усиление внеклеточного сигнала на этом этапе (рис. 5-35).

Рис. 5-35. Цикл функционирования G-белка. R s - рецептор; Г - гормон; АЦ - аденилатциклаза.
Активированная α-субъединица G-белка (α-ГТФ) взаимодействует со специфическим белком клеточной мембраны и изменяет его активность. Такими белками могут быть ферменты аденилатциклаза, фосфолипаза С, фосфодиэстераза цГМФ, Na + -каналы, К + -каналы.
Следующий этап цикла функционирования G-белка - дефосфорилирование ГТФ, связанного с α-субъединицей, причём фермент, катализирующий эту реакцию, - сама α-субъединица.
Дефосфорилирование приводит к образованию комплекса α-ГДФ, который не комплементарен специфическому белку мембраны (например, аденилатциклазе), но имеет высокое сродство к βγ-протомерам. G-белок возвращается к неактивной форме - αβγ-ГДФ. При последующей активации рецептора и замене молекулы ГДФ на ГТФ цикл повторяется снова. Таким образом, α-субъединицы G-белков совершают челночное движение, перенося стимулирующий или ингибирующий сигнал от рецептора, который активирован первичным посредником (например, гормоном), на фермент, катализирующий образование вторичного посредника.
Некоторые формы протеинкиназ могут фосфорилировать α-субъединицы G-белков. Фосфорилированная α-субъединица не комплементарна специфическому белку мембраны, например, аденилатциклазе или фосфолипазе С, поэтому не может участвовать в передаче сигнала.
Г. аденилатциклаза
Фермент аденилатциклаза, катализирующий превращение АТФ в цАМФ (рис. 5-36), - ключевой фермент аденилатциклазной системы передачи сигнала. Аденилатциклаза обнаружена во всех типах клеток.

Рис. 5-36. Образование циклического аденозинмонофосфата (цАМФ).
Фермент относят к группе интегральных белков клеточной мембраны, он имеет 12 трансмембранных доменов. Внеклеточные фрагменты аденилатциклазы гликозилированы. Цитоплазматические домены аденилатциклазы имеют два каталитических центра, ответственных за образование цАМФ - вторичного по средника, участвующего в регуляции активности фермента протеинкиназы А.
На активность аденилатциклазы оказывают влияние как внеклеточные, так и внутриклеточные регуляторы. Внеклеточные регулятор (гормоны, эйкозаноиды, биогенные амины) осуществляют регуляцию через специфические рецепторы, которые с помощью α-субъединиц G-белков передают сигналы на аденилатциклазу. αs - Субъединица (стимулирующая) при взаимодействии с аденилатциклазой активирует фермент, αi- Субъединица (ингибирующая) ингибирует фермент. В свою очередь, аденилатциклаза стимурирует проявление ГТФ- фосфотазной активности α- субъединиц. В результате дефосфорилирования ГТФ образуются субъединицы а s -ГДФ и а i -ГДФ, не комплементарные аденилатциклазе.
Из 8 изученных изоформ аденилатциклазы 4 - Са 2+ -зависимые (активируются Са 2+). Регуляция аденилатциклазы внутриклеточным кальцием позволяет клетке интегрировать активность двух основных вторичных посредников цАМФ и Са 2+ .
Д. фосфолипазы
Фосфолипазы - ферменты класса гидролаз, катализирующие катаболизм глицерофосфолипидов. Различают фосфолипазы секреторные, входящие в состав панкреатического сока, и клеточные фосфолипазы. Клеточные фосфолипазы А 1 , А 2 , D, С различаются по специфичности к отщепляемой группе. Все фосфолипазы - кальций зависимые ферменты (рис. 5-37).

Рис. 5-37. Действие фосфолипаз.
Фосфолипаза С - фермент, гидролизующий фосфоэфирную связь в глицерофосфолипидах. В клетках человека идентифицировано 10 изоформ фосфолипазы С, различающихся по молекулярной массе, локализации, способу регуляции, субстратной специфичности. В структуре всех изоформ фосфолипазы С отсутствуют гидрофобные домены, которые могли бы обеспечить их взаимодействие с мембраной. Однако некоторые формы фосфолипазы С связаны с помощью гидрофобного «якоря» - ацильного остатка миристиновой кислоты или за счёт взаимодействия с поверхностью бислоя. Каталитическая активность всех изоформ фосфолипазы С зависит от ионов кальция.
Большинство фосфолипаз С специфично в отношении фосфатидилинозитолов и практически не гидролизует другие типы фосфолипидов. Активный фермент может гидролизовать до 50% от общего количества фосфатидилинозитолов клеточной мембраны. При гидролизе фосфатидилинозитол-4,5-бисфосфата (ФИФ 2) образуются продукты диацилглицерол (ДАГ) и инозитол-1,4,5-трифосфат (ИФ 3), служащие вторичными посредниками в трансмембранной передаче сигнала по инозитолфосфатному пути.
Е. протеинкиназы
Все полярные сигнальные молекулы, действующие на клетку-мишень через мембранные рецепторы, осуществляют свою биологическую функцию путём фосфорилирования специфических белков и ферментов, регулирующих метаболизм в клетке. Фосфорилирование изменяет (увеличивает или уменьшает) их активность. Катализируют фосфорилирование белков (протеинов) протеинкиназы по аминокислотным остаткам серина, треонина, тирозина. Протеинкиназы могут быть субъединицей мембранного рецептора, например тирозиновая протеинкиназа рецептора инсулина, активность которой регулируется гормоном. Другая группа - протеинкиназы, регулируемые вторичными вестниками гормонального сигнала (цАМФ, цГМФ, Са 2+ , ДАГ), например протеинкиназа А, протеинкиназа С, протеинкиназа G, кальмодулинзависимые протеинкиназы и др.
Протеинкиназы А
Протеинкиназы А (цАМФ-стимулируемые) участвуют в аденилатциклазной системе передачи сигнала. Протеинкиназа А состоит из 4 субъединиц R 2 С 2 - двух регуляторных субъединиц (R 2) и двух каталитических (С 2) (см. рис. 5-41). Комплекс R 2 С 2 не обладает ферментативной активностью.
Комплекс R 2 С 2 разными способами прикрепляется к мембране. Некоторые формы протеинкиназы А «заякориваются» с помощью алифатического остатка миристиновой кислоты каталитических субъединиц. Во многих тканях протеинкиназа А связана с «заякоренным» белком АКАР s (от англ. сАМР dependent protein kinase anchoring proteins). АКАР s имеет центр связывания для регуляторных субъединиц протеинкиназы А. С помощью белка АКАР s протеинкиназа А связывается с мембраной в области локализации ферментов, катализирующих образование цАМФ (аденилатциклаза) или его гидролиз (фосфодиэстераза), а также белков, в регуляции активности которых фермент принимает участие, например потенциалзависимые Са 2+ -каналы.
Регуляторные субъединицы протеинкиназы А имеют специфические центры для связывания цАМФ. Присоединение цАМФ к регуляторным, субъединицам приводит к изменению конформации последних и снижению сродства к каталитическим субъединицам С, происходит диссоциация по схеме:
цАМФ 4 + R 2 С 2 -> цАМФ 4 R 2 + С + С
Субъединицы С представляют собой активную форму протеинкиназы А, которая катализирует реакции фосфорилирования по серину и треонину. Каталитические субъединицы С у разных типов протеинкиназ а не идентичны, они различаются прежде всего специфичностью в отношении белков-субстратов.
Протеинкиназы С
Протеинкиназы С участвуют в инозитолфосфатной системе передачи сигнала. Фермент состоит из двух функционально различных доменов - регуляторного и каталитического. Регуляторный домен содержит 2 структуры («цинковые пальцы»), образованные фрагментами пептидной цепи, богатыми цистеином, и содержащими 2 иона цинка (см. раздел 1). «Цинковые пальцы» участвуют в связывании диацилглицерола. Другой фрагмент регуляторного домена имеет высокое сродство к Са 2+ . Повышение концентрации кальция в цитозоле увеличивает сродство протеинкиназы С к фосфатидилсерину мембраны. Транслокация протеинкиназы С к мембране позволяет ферменту связаться с ДАГ, который ещё больше повышает сродство протеинкиназы С к ионам кальция (рис. 5-38). Наиболее распространённые изоформы протеинкиназы С активируются Са 2+ , диацилглицеролом и фосфатидилсерином.

5-38. Регуляция активности протеинкиназы С (ПКС). ФС - фосфатидилсерин; ДАГ - диаципглицерол.
Каталитический домен имеет центр, связывающий АТФ и белок-субстрат. Активная фермента протеинкиназы С фосфорилирует по остаткам серина и треонина. Снижение концентрации ионов кальция в клетке нарушает связь протеинкиназы С с фосфатидилсерином и диацилглицеролом, фермент переходит в неактивную форму и отделяется от мембраны.
3. Протеинкиназы G
В отличие от протеинкиназы А, протеинкиназа G присутствует не во всех тканях, ее обнаруживают в лёгких, мозжечке, гладких мышцах и тромбоцитах. Изоформы протеинкиназы G могут быть связаны с мембраной или находиться цитоплазме. Растворимая протеинкиназа С состоит из двух идентичных субъединиц, каждая из которых имеет два центра для связывания цГМФ. Приединение цГМФ к регуляторным центрам вызывает конформационные изменения субъединиц и повышает каталитическую активность фермента (рис. 5-39). Протеинкиназа G, подобно протеинкиназе А и С, специфична в отношении определённых белковых субстратов, которые она фосфорилирует по остаткам серина и треонина.

Рис. 5-39. Регуляция активности протеинкиназы G (ПКG).
Ж фосфодиэстеразы
Фосфодиэстеразы - ферменты, катализирующие превращение цАМФ (рис. 5-40) или цГМФ в неактивные метаболиты АМФ или ГМФ. Фосфодиэстеразы, снижая концентрации вторичных посредников, разрывают цепь превращений, вызванных активатором рецептора.

Рис.5-40. Превращение цАМФ в АМФ.
Фосфодиэстеразы присутствуют в клетках тканей в 2 формах: в форме растворимого белка и мембранносвязанного. Формы фермента, связанные с мембраной, в разных тканях составляют 5-40%. В одной и той же ткани могут присутствовать разные формы фосфодиэстеразы, различающиеся по сродству к субстратам, молекулярному весу, заряду, регуляторным свойствам и локализации в клетке.
Фосфодиэстеразы циклических нуклеотидов не обладают абсолютной специфичностью, поэтому, как правило, одна и та же форма фермента способна гидролизовать как цАМФ, так и цГМФ. Однако скорости гидролиза этих двух нуклеотидов под действием одной и той же фосфодиэстеразы могут значительно различаться. Это зависит от того, какая фосфодиэстераза присутствует в клетке - более специфичная в отношении цАМФ или более специфичная к цГМФ, от соотношения концентраций цАМФ и цГМФ в клетке и от действия регуляторов фосфодиэстеразы.
В большинстве тканей присутствует фосфодиэстераза-1, более специфичная к цАМФ, активируемая Са 2+ , комплексом 4 Са 2+ -кальмодулин и цГМФ.








 Внедрение и использование УМК «Изучаем русский язык» в двуязычной образовательной среде
Внедрение и использование УМК «Изучаем русский язык» в двуязычной образовательной среде Система образования в индии как фундамент знаний и жизни
Система образования в индии как фундамент знаний и жизни Роман Вишневский – трейдер и владелец брокерской компании
Роман Вишневский – трейдер и владелец брокерской компании Николай Кольцов – биолог из будущего
Николай Кольцов – биолог из будущего